Karbamidas: Skirtumas tarp puslapio versijų
S robotas Pridedama: bn:ইউরিয়া |
S robotas Pridedama: bs:Urea; smulkūs taisymai |
||
| Eilutė 13: | Eilutė 13: | ||
| InChI = |
| InChI = |
||
| tankis ir būsena = 1,33·10³ kg/m³ |
| tankis ir būsena = 1,33·10³ kg/m³ |
||
| tirpumas =108 g/100 ml (20 |
| tirpumas =108 g/100 ml (20 °C)<br />167 g/100 ml (40 °C)<br />251 g/100 ml (60 °C)<br />400 g/100 ml (80 °C)<br />733 g/100 ml (100 °C) |
||
| lužio rodiklis = |
| lužio rodiklis = |
||
| lydymosi temp = 132,7 |
| lydymosi temp = 132,7 °C (susiskaido) |
||
| virimo temp = - |
| virimo temp = - |
||
| rūgštingumas = 26,9 |
| rūgštingumas = 26,9 |
||
| Eilutė 40: | Eilutė 40: | ||
}} |
}} |
||
'''Karbamidas, šlapalas, urėja''', '''anglies rūgšties diamidas''' – bespalviai, bekvapiai tetragoninės singonijos šaldančio skonio kristalai. Gerai tirpsta [[vanduo|vandenyje]], [[etilo alkoholis|etilo alkoholyje]], skystame [[amoniakas|amoniake]]. |
'''Karbamidas, šlapalas, urėja''', '''anglies rūgšties diamidas''' – bespalviai, bekvapiai tetragoninės singonijos šaldančio skonio kristalai. Gerai tirpsta [[vanduo|vandenyje]], [[etilo alkoholis|etilo alkoholyje]], skystame [[amoniakas|amoniake]]. |
||
<br />Kaitinant 150–160°C temperatūroje atskyla amoniakas ir karbamidas virsta [[ciano rūgštis|ciano rūgštimi]]; pastaroji iš dalies polimerizuojasi, sudarydama biuretą. Šildomas vandeninis karbamido tirpalas išskiria NH<sub>3</sub> ir CO<sub>2</sub>. Reaguodamas su [[nitritinė|nitritine]] [[rūgštis|rūgštimi]], išskiria [[azotas|azotą]]: |
<br />Kaitinant 150–160 °C temperatūroje atskyla amoniakas ir karbamidas virsta [[ciano rūgštis|ciano rūgštimi]]; pastaroji iš dalies polimerizuojasi, sudarydama biuretą. Šildomas vandeninis karbamido tirpalas išskiria NH<sub>3</sub> ir CO<sub>2</sub>. Reaguodamas su [[nitritinė|nitritine]] [[rūgštis|rūgštimi]], išskiria [[azotas|azotą]]: |
||
: <math>\mathrm{\ (NH_2)_2CO + 2HNO_2 \ \longrightarrow \ 2N_2 + CO_2 + 3H_2O}</math> |
: <math>\mathrm{\ (NH_2)_2CO + 2HNO_2 \ \longrightarrow \ 2N_2 + CO_2 + 3H_2O}</math> |
||
Su [[azotas|azoto]], [[druska|druskos]], [[fosforas|forsforo]], [[Oksalo rūgštis|oksalo rūgštimis]] sudaro druskas. Alkilinamas karbamidas sudaro alkilkarbamidą R-NHCONH<sub>2</sub>, acilinamas – ureidus RCO-NHCONH<sub>2</sub>, reaguodamas su alkoholiais - uretanus N<sub>2</sub>NCOOR (čia R – angliavandenilio radikalas), su [[parafinai]]s ir jų dariniais, pvz., aukštesniaisiais [[alkoholis|alkoholiais]], [[rūgštis|rūgštimis]], [[esteriai]]s, halogenidais ir nitrilais, sudaro kristališkuosius aduktus. Laboratorijoje gaunamas iš kalio arba natrio cianato ir amonio chlorido arba cianamino hidrolize, pramonėje – iš amoniako ir anglies dioksido: |
Su [[azotas|azoto]], [[druska|druskos]], [[fosforas|forsforo]], [[Oksalo rūgštis|oksalo rūgštimis]] sudaro druskas. Alkilinamas karbamidas sudaro alkilkarbamidą R-NHCONH<sub>2</sub>, acilinamas – ureidus RCO-NHCONH<sub>2</sub>, reaguodamas su alkoholiais - uretanus N<sub>2</sub>NCOOR (čia R – angliavandenilio radikalas), su [[parafinai]]s ir jų dariniais, pvz., aukštesniaisiais [[alkoholis|alkoholiais]], [[rūgštis|rūgštimis]], [[esteriai]]s, halogenidais ir nitrilais, sudaro kristališkuosius aduktus. Laboratorijoje gaunamas iš kalio arba natrio cianato ir amonio chlorido arba cianamino hidrolize, pramonėje – iš amoniako ir anglies dioksido: |
||
| Eilutė 52: | Eilutė 52: | ||
[[bg:Карбамид]] |
[[bg:Карбамид]] |
||
[[bn:ইউরিয়া]] |
[[bn:ইউরিয়া]] |
||
[[bs:Urea]] |
|||
[[ca:Urea]] |
[[ca:Urea]] |
||
[[cs:Močovina]] |
[[cs:Močovina]] |
||
02:22, 17 rugsėjo 2009 versija
| Karbamidas | |
|---|---|
 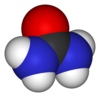
| |
| Sisteminis (IUPAC) pavadinimas | |
| CAS numeris | [57-13-6] |
| Cheminė formulė | (NH2)2CO |
| Molinė masė | 60,07 g/mol |
| SMILES | NC(=O)N |
| Rūgštingumas (pKa) | 26,9 |
| Bazingumas (pKb) | 13,82 |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | bespalviai, bekvapiai kristalai |
| Lydymosi t° | 132,7 °C (susiskaido) |
| Virimo t° | - |
| Lūžio rodiklis (nD) | |
| Klampumas | |
| Tirpumas H2O | 108 g/100 ml (20 °C) 167 g/100 ml (40 °C) 251 g/100 ml (60 °C) 400 g/100 ml (80 °C) 733 g/100 ml (100 °C) |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | Toksiškas (T) |
| NFPA 704 | |
| Žybsnio t° | |
| Užsiliepsnojimo t° | |
| R-frazės | |
| S-frazės | |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
| Molekulinė forma | |
| Dipolio momentas | 4,56 p/D |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
|
| Giminingi junginiai | |
| Giminingi grupė | |
| Giminingi junginiai | |
| Giminingos grupės | |
Karbamidas, šlapalas, urėja, anglies rūgšties diamidas – bespalviai, bekvapiai tetragoninės singonijos šaldančio skonio kristalai. Gerai tirpsta vandenyje, etilo alkoholyje, skystame amoniake.
Kaitinant 150–160 °C temperatūroje atskyla amoniakas ir karbamidas virsta ciano rūgštimi; pastaroji iš dalies polimerizuojasi, sudarydama biuretą. Šildomas vandeninis karbamido tirpalas išskiria NH3 ir CO2. Reaguodamas su nitritine rūgštimi, išskiria azotą:
Su azoto, druskos, forsforo, oksalo rūgštimis sudaro druskas. Alkilinamas karbamidas sudaro alkilkarbamidą R-NHCONH2, acilinamas – ureidus RCO-NHCONH2, reaguodamas su alkoholiais - uretanus N2NCOOR (čia R – angliavandenilio radikalas), su parafinais ir jų dariniais, pvz., aukštesniaisiais alkoholiais, rūgštimis, esteriais, halogenidais ir nitrilais, sudaro kristališkuosius aduktus. Laboratorijoje gaunamas iš kalio arba natrio cianato ir amonio chlorido arba cianamino hidrolize, pramonėje – iš amoniako ir anglies dioksido:
Karbamidas – žmogaus ir daugumos žinduolių gyvūnų baltymų apykaitos galutinis produktas. Gaminasi kepenyse. Randamas kraujyje (normaliai 18–38 mg/100ml), raumenyse ir kituose audiniuose, seilėse, limfoje, piene. Reguliuoja vandens apykaitą organizme, audinių hidrataciją. Šalinamas pro inkstus ir prakaito liaukas. Sutrikus inkstų funkcijai ir skylant audinių baltymams karbamido daugėja kraujyje (uremija), dirbant sunkų fizinį darbą, sergant cukriniu diabetu, karščiuojant – šlapime.



