Anglis
| |
Šiam straipsniui ar jo daliai reikia daugiau nuorodų į patikimus šaltinius. Jūs galite padėti Vikipedijai įrašydami tinkamas išnašas ar nuorodas į patikimus šaltinius. |
 Kitos reikšmės – Anglis (reikšmės).
Kitos reikšmės – Anglis (reikšmės).
| Anglis (C) | |
|---|---|
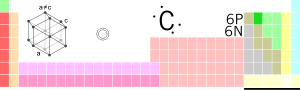
| |
| Periodinė grupė |
Nemetalas |
| Atomo numeris | 6 |
| Išvaizda | |
| Atomo savybės | |
| Atominė masė (Molinė masė) |
12,0107(8) а.m.v. (g/mol) |
| Atomo spindulys |
91 pm |
| Jonizacijos energija (pirmas elektronas) |
1086,5 kJ/mol (eV) |
| Elektronų konfigūracija | (11.3 eV)
1s² 2s² 2p² |
| Cheminės savybės | |
| Kovalentinis spindulys |
77 pm |
| Jono spindulys |
? pm |
| Elektroneigiamumas |
2,55 (pagal Polingą) |
| Elektrodo potencialas |
? |
| Oksidacijos laipsniai |
-4, +2, +4 |
| Termodinaminės savybės | |
| Tankis |
2,26 g/cm³ |
| Šiluminė talpa |
? J/(K·mol) |
| Šiluminis laidumas |
155 W/(m·K) |
| Lydymosi temperatūra |
3825 K |
| Lydymosi šiluma |
20,28 kJ/mol |
| Virimo temperatūra |
5100 K |
| Garavimo šiluma |
715 kJ/mol |
| Molinis tūris |
5,31 cm³/mol |
| Kristalinė gardelė | |
| Kristalinė gardelė |
? |
| Gardelės periodas |
? Å |
Anglis (Carbonium) – cheminis periodinės elementų lentelės elementas, žymimas C, eilės numeris 6.[1]
Atomų masė 12,01115. Išorinių elektronų konfigūracija 2s²2p². Oksidacijos laipsnis junginiuose +2, +4, -4. Stabilūs izotopai 12C (98,892 %) ir 13C (1,108 %). Kosminiai spinduliai dalį atmosferos azoto paverčia radioaktyviu anglies izotopu 14C (pusėjimo trukmė 5730 metų). Izotopo 12C masės 1 / 12 dalis – cheminių elementų atomų masės vienetas. Anglis sudaro 0,023 % Žemės plutos masės. Organinių junginių pavidalu anglies yra visų organizmų audiniuose, akmens ir rusvosiose anglyse, durpėse, naftoje, gamtinėse dujose. 0,03 % (pagal tūrį) atmosferos sudaro anglies dioksidas CO2. Anglies yra gamtiniuose metalų karbonatuose (klintyje, kreidoje, marmure, dolomite, magnezite).
Charakteristikos[redaguoti | redaguoti vikitekstą]
Yra 8 anglies alotropinės atmainos: amorfinė anglis, grafitas, deimantas, anglies nanovamzdeliai, fulerenas ir sintetinė – karbinas. Amorfinė anglis – suodžiai – juodi milteliai; grafitas – pilkai juodos spalvos kristalai, sistema heksagonalinė, kietumas 1, tankis 2230 kg/m³. Deimantas – bespalviai skaidrūs kristalai, sistema kubinė, kietumas 10, tankis 3510 kg/m³. Aukštoje temperatūroje (apie 1500 °C) deimantas ir grafitas virsta karbinu.
Visų anglies modifikacijų lydymosi temperatūra 3500–3700 °C. Anglis – nemetalas. Tirpsta išlydytuose metaluose, pvz., geležyje, kobalte, nikelyje. Degdama sudaro anglies dioksidą (jei deguonies netrūksta) ir anglies monoksidą (jei deguonies trūksta). Kaitinama su metalais ar jų oksidais, sudaro karbidus; pvz., iš anglies ir aliuminio oksido gaunamas aliuminio karbidas: 9C + 2Al2O3 → Al4C3 + 6CO. Aukštoje temperatūroje jungiasi su halogenais (pvz., su chloru sudaro anglies tetrachloridą CCl4), siera ir kitais elementais. Anglies yra visuose organiniuose junginiuose. Didžiausios organiniu junginių grupės yra angliavandeniliai ir angliavandeniai. Anglies atomai gali sudaryti linijines, šakotas grandines ir žiedus, prie kurių prisijungę vandenilio, deguonies ir kitų elementų atomai. Šiose grandinėse anglies atomų jungtys yra viengubos, dvigubos ir trigubos. Dvigubas jungtis turinčios molekulės linkusios stambėti (polimerizuotis) – susidaro stambiamolekuliai junginiai.
Panaudojimas[redaguoti | redaguoti vikitekstą]
Anglis ir jos gamtiniai junginiai – svarbus energijos šaltinis ir chemijos pramonės žaliava. Iš grafito daromi elektrodai, gaunamos raketinių variklių antikorozinės dangos, grafito plastikai, juo futeruojama cheminė aparatūra. Labai grynu dirbtiniu grafitu atominiuose reaktoriuose lėtinami neutronai. Šlifuoti deimantai vartojami papuošalams. Iš deimanto gaminamos gręžimo įrankių vainikėliai. Suodžiai vartojami gumos gamyboje kaip užpildas.
Istorija[redaguoti | redaguoti vikitekstą]
Didelės molekulinės masės anglies junginiai evoliucijos metu sudarė gyvybės atsiradimo Žemėje pamatą. Augalų ląstelės geba asimiliuoti atmosferos anglies dioksidą. Iš šio gebėjimo atsirado chemosintezė, fotoredukcija ir fotosintezė.
Biologinė reikšmė[redaguoti | redaguoti vikitekstą]
Augaluose anglis sudaro 42-45 % sausosios masės, gyvūnuose 0,1-26 % gyvosios masės. Tos pačios rūšies organizmuose anglies kiekis priklauso nuo lyties, amžiaus, vystymosi stadijos ir kitų sąlygų. Svarbiausias žaliųjų augalų anglies šaltinis (95-98 %) yra atmosferos anglies dioksidas, gyvūnų – augalų susintetinti organiniai anglies junginiai. Žuvus organizmams, didžioji jų kūno dalis virsta anglies dioksidu. Dalis augalų asimiliuotos anglies ilgainiui virsta durpėmis, akmens anglimis, nafta, dujomis, dirvos humusu, sapropeliu. Be stabiliosios anglies 12C, augaluose kaupiasi ir radioaktyvioji 14C. Su maistu ji patenka į gyvūnų ir žmogaus organizmą. Radioaktyviosios anglies kiekis augalų ir gyvūnų liekanose rodo, kada jie gyveno. Radioaktyvioji anglis naudojama fotosintezei, medžiagų kitimui ir apytakai organizme tirti. Bakterijų, virusų, vabzdžių žymėjimas radioaktyviąja anglimi padeda tirti jų biologiją, kovoti su ligų sukėlėjais, augalų ir gyvūnų kenkėjais.
Šaltiniai[redaguoti | redaguoti vikitekstą]
- ↑ Danutė Ona Kimtienė, Arvydas Markuckas. Anglis (lot. Carboneum). Visuotinė lietuvių enciklopedija, T. I (A-Ar). – Vilnius: Mokslo ir enciklopedijų leidybos institutas, 2001. 521-522 psl.

