Natrio hidrokarbonatas
| Natrio hidrokarbonatas | |
|---|---|
| |
| Sisteminis (IUPAC) pavadinimas | |
| Natrio hidrokarbonatas | |
| CAS numeris | [144-55-8] |
| RTECS numeris | VZ0950000 |
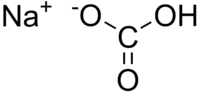
| Cheminė formulė | NaHCO3 |
| Molinė masė | 84,007 g/mol |
| SMILES | C(=O)(O)[O-].[Na+] |
| Rūgštingumas (pKa) | 6.3 |
| Bazingumas (pKb) | |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | Balti milteliai |
| Lydymosi t° | skyla |
| Virimo t° | skyla |
| Lūžio rodiklis (nD) | |
| Klampumas | |
| Tirpumas H2O | 7.8 g/100 g (18 °C) |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | |
| NFPA 704 | |
| Žybsnio t° | nedegus |
| Užsiliepsnojimo t° | |
| R-frazės | |
| S-frazės | |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
| Molekulinė forma | |
| Dipolio momentas | |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
|
| Giminingi junginiai | |
| Giminingi druskos | kalio hidrokarbonatas, kalcio hidrokarbonatas |
| Giminingi junginiai | natrio karbonatas |
| Giminingos grupės | |

Natrio hidrokarbonatas NaHCO3 (kiti pavadinimai: natrio bikarbonatas, kepimo milteliai, kepimo soda, maistinė soda[1] ) – natrio ir angliarūgštės druska.
Natrio hidrokarbonatas – balti kristaliniai milteliai, be kvapo. Jis šiek tiek sūrus, šarminiu skoniu primenantis skalbiamąją sodą (natrio karbonatas). E numeris – E500.[2] Natrio hidrokarbonatas gaunamas kaip vienas iš tarpinių Solvejaus proceso produktų (pagrindinis produktas yra natrio karbonatas). Jo tirpalas dėl hidrolizės turi silpnai šarminę reakciją. Gamtoje kartais aptinkamas kaip mineralas nahcolitas.[3]
Skilimai[redaguoti | redaguoti vikitekstą]
Natrio hidrokarbonatas naudojamas kepinio (kekso, duonos, pyrago) struktūros suformavimui reikalingoms dujoms pagaminti. Esant rūgščiai aplinkai, natrio hidrokarbonatas skyla:[4]
- NaHCO3 + H+ → Na+ + CO2 + H2O
Galimas taip pat terminis skilimas, nors jis ne tiek naudingas, nes dujų pagaminama nedaug.[4] Terminis skilimas prasideda virš 70 °C , greitai reakcijai reikia apie 200 °C:
- 2NaHCO3 → Na2CO3 + H2O + CO2
Toliau kaitinamas ties 1000 °C, natrio karbonatas skyla į natrio oksidą ir anglies dioksidą:
- Na2CO3 → Na2O + CO2
Dėl šių virsmų natrio hidrokarbonatas naudojamas, kaip ugnies gesinimo reagentas (BC klasės gaisrams), kai kurių sausų miltelių gesintuvuose.
Natrio hidrokarbonatas tai pat naudojamas neutralizuoti skrandžio rūgšties pertekliui, vaistų gamyboje ir pan. Taip pat jis yra naudojamas gazuoto vandens gamyboje.
Šaltiniai[redaguoti | redaguoti vikitekstą]
- ↑ „What's the difference between bicarbonate of soda, baking soda and baking powder?“. ThatsLife! Pacific Network.
- ↑ „Approved additives and E numbers“. Food Standards Agency (anglų). Nuoroda tikrinta 7 December 2020.
- ↑ Nahcolite data on Webmineral
- ↑ 4,0 4,1 Bent AJ, red. (1997). The Technology of Cake Making (6 leid.). Springer. p. 102. ISBN 9780751403497. Nuoroda tikrinta 12 August 2009.

