Diazoto monoksidas
| Diazoto monoksidas | |
|---|---|
  | |
| Sisteminis (IUPAC) pavadinimas | |
| CAS numeris | [10024-97-2] |
| PubChem | 948 |
| Cheminė formulė | N2O |
| Molinė masė | 44,0128 g/mol |
| SMILES | [N+]([O-])#N |
| Rūgštingumas (pKa) | |
| Bazingumas (pKb) | |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | bespalvės dujos |
| Lydymosi t° | -90,86 °C (182,29 K) |
| Virimo t° | -88,48 °C (184,67 K) |
| Lūžio rodiklis (nD) | |
| Klampumas | |
| Tirpumas H2O | |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | 0,004 % |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | |
| NFPA 704 | |
| Žybsnio t° | |
| Užsiliepsnojimo t° | |
| R-frazės | R8 |
| S-frazės | S38 |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
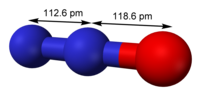
| Molekulinė forma | linijinė |
| Dipolio momentas | 0,166D |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
+82,05 |
| Giminingi junginiai | |
| Giminingi grupė | |
| Giminingi junginiai | Azoto monoksidas, Azoto dioksidas, Diazoto trioksidas, Diazoto tetroksidas, Diazoto pentaoksidas, Azoto rūgštis, Nitrozilo hidroksidas |
| Giminingos grupės | |
Diazoto oksidas arba diazoto monoksidas – dujos, sudarytos iš dviejų azoto ir vieno deguonies atomų. Tai bespalvės ir praktiškai bekvapės dujos. Pats azoto oksidas – nedegus. Šios dujos nėra toksiškos, nesukelia alerginių reakcijų, įkvėptos mažomis dozėmis gali sukelti isteriją ar nekontroliuojamą juoko priepuolį, dėl ko dar vadinamos juoko dujomis. Dujos veikia atpalaiduojančiai ir migdančiai, dėl to seniau buvo naudojamos medicinoje kaip anestezijos priemonė. Nuo 1970-ųjų šias dujas imta taikyti pramonėje: aviacijoje ir autotechnikoje.
Gavimas[redaguoti | redaguoti vikitekstą]
Diazoto monoksidas yra gaunamas 170–195 °C termiškai skaidant sausąjį amonio nitratą:[1]
Azoto oksidas variklyje[redaguoti | redaguoti vikitekstą]
Į variklį azoto oksidas atneša daugiau deguonies, todėl degalai greičiau dega ir suteikia varikliui didesnę galią. 300° C temperatūtoje, kokia yra cilindre uždegimo metu, diazoto monoksidas skyla į azoto ir deguonies dujas. Tai gerokai padidina slėgį deguonies ir degalų mišinyje virš normalaus slėgio, kuris būdingas Žemės atmosferai. Būtent dėl šios priežasties degalai sudega greičiau. Be to, irimo reakcijos metu išsiskyręs azotas sušvelnina padidėjusį spaudimą cilindre valdydamas degimą: diazoto monoksido savitoji garavimo šiluma sumažina įsiurbimo temperatūrą.
Šaltiniai[redaguoti | redaguoti vikitekstą]
- ↑ ŽARNAUSKAS Algirdas, ANCUTIENĖ Ingrida, IVANAUSKAS Remigijus, PETRAŠAUSKIENĖ Neringa. Neorganinė chemija. Kaunas: Technologija, 2008, 197 p. ISBN 978-9955-25-519-2.


