Kalio šarmas
Išvaizda
(Nukreipta iš puslapio E525)
| |
Šiam straipsniui ar jo daliai trūksta išnašų į patikimus šaltinius. Jūs galite padėti Vikipedijai pridėdami tinkamas išnašas su šaltiniais. |
| Kalio šarmas | |
|---|---|
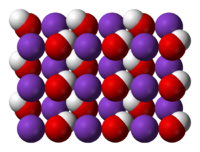
| |
| Sisteminis (IUPAC) pavadinimas | |
| Kalio hidroksidas | |
| CAS numeris | 1310-58-3 |
| PubChem | 6093213 |
| ChemSpider | 14113 |
| RTECS numeris | TT2100000 |
| Cheminė formulė | KOH |
| Molinė masė | 56,10564 g/mol |
| SMILES | [OH-].[K+] |
| Rūgštingumas (pKa) | -2,29 |
| Bazingumas (pKb) | |
| Valentingumas | |
| Fizinė informacija | |
| Tankis | |
| Išvaizda | balta kieta medžiaga |
| Lydymosi t° | 406 °C |
| Virimo t° | 1320 °C |
| Lūžio rodiklis (nD) | 1,409 |
| Klampumas | |
| Tirpumas H2O | 110 g/100 mL (25 °C) 178 g/100 mL (100 °C) |
| Šiluminis laidumas | |
| log P | |
| Garavimo slėgis | |
| kH | |
| Kritinis santykinis drėgnumas | |
| Farmakokinetinė informacija | |
| Biotinkamumas | |
| Metabolizmas | |
| Pusamžis | |
| Pavojus | |
| MSDS | |
| ES klasifikacija | Sukelia koroziją (C) |
| NFPA 704 | |
| Žybsnio t° | nedegus |
| Užsiliepsnojimo t° | |
| R-frazės | R22, R35 |
| S-frazės | S1/2, S26, S36/37/39, S45 |
| LD50 | |
| Struktūra | |
| Kristalinė struktūra | |
| Molekulinė forma | |
| Dipolio momentas | |
| Simetrijos grupė | |
| Termochemija | |
| ΔfH |
|
| Giminingi junginiai | |
| Giminingi šarmai | natrio šarmas, kalcio hidroksidas |
| Giminingi junginiai | kalio chloridas |
| Giminingos grupės | |
Kalio šarmas arba kalio hidroksidas (KOH) – stipri bazė. Tai – balta, kieta medžiaga. Tyžta ore.
Kalio šarmas gaunamas elektrolizuojant kalio chlorido vandeninį tirpalą.
Naudojamas skysto muilo gamyboje, dirvų rūgštingumui mažinti, įvairių kalio junginių gavimui ir pan.
Gamyba
[redaguoti | redaguoti vikitekstą]Istoriškai KOH buvo gaminamas pridedant kalio karbonato (potašo) į stiprų kalcio hidroksido tirpalą (gesintas kalkes), įvykusios reakcijos metu kalcio karbonatas nusėda, palikdamas kalio hidroksidą tirpale:
- Ca(OH)2 + K2CO3 → CaCO3 + 2 KOH
Kalcio karbonato išfiltravimas ir išvirimas iki tirpalo pagamina kalio hidroksidą. Tai buvo pats svarbiausias kalcio hidroksido gamybos būdas iki vėlyvojo XIX a., kai jį pakeitė dabartinis elektrolizės metodas. Šis metodas yra analogiškas natrio hidroksido gamybai:
- 2 KCl + 2 H2O → 2 KOH + Cl2 + H2


